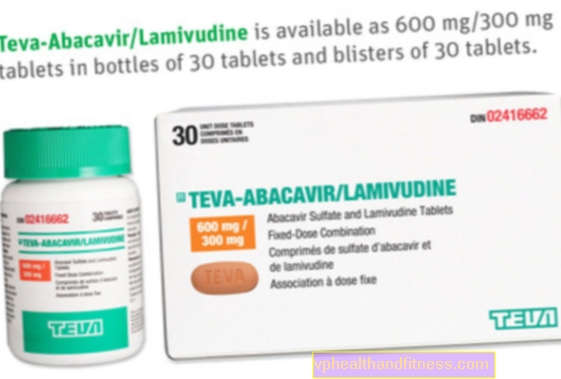
1タブレット捕虜。アバカビル600mgとラミブジン300mgが含まれています。
| 名前 | パッケージの内容 | 活性物質 | 価格100% | 最終更新日 |
| アバカビル/ラミブジンテバ | 30個(ブリスター)、テーブル捕虜。 | ラミブジン、 アバカビル | 2019-04-05 |
アクション
アバカビルとラミブジンは、ヌクレオシド系逆転写酵素阻害剤(NRTI)であり、HIV-1およびHIV-2複製の強力な選択的阻害剤です。アバカビルとラミブジンの両方は、細胞内キナーゼによって対応する5'-三リン酸(TP)に順次代謝されます。ラミブジン三リン酸、カルボビル三リン酸(アバカビルの活性三リン酸型)は基質であり、HIV逆転写酵素の競合阻害剤でもあります。それらの抗ウイルス活性の主なメカニズムは、ウイルスDNA鎖への一リン酸の付着であり、複製の完了をもたらします。アバカビルおよびラミブジン三リン酸は、宿主細胞DNAポリメラーゼに対して有意に低い親和性を示します。ラミブジンと他の抗レトロウイルス薬であるジダノシン、ネビラピンおよびジドブジンの間には拮抗的な相互作用は観察されていません。細胞培養におけるアバカビルの抗ウイルス活性は、薬物をヌクレオシド逆転写酵素阻害剤(NRTI)と組み合わせて使用した場合、拮抗されませんでした:ジダノシン、エムトリシタビン、スタブジン、テノホビルまたはジドブジン、非ヌクレオシド逆転写酵素阻害剤(NNRTIまたはネビラプロターゼ阻害剤)(NNRTI)。 -アンプレナビル。アバカビルとラミブジンの組み合わせ錠は、ラミブジンとアバカビルを単独で投与した場合と生物学的に同等です。アバカビルとラミブジンは、経口投与後、消化管から迅速かつ良好に吸収されます(バイオアベイラビリティ-アバカビルでは83%、ラミブジンでは80-85%)。アバカビルとラミブジンの薬物濃度がピークになるまでの時間の中央値は、それぞれ約1.5時間と1時間です。ラミブジンは血漿タンパク質への結合が不十分です(<36%)。アバカビルは、肝臓でアルコールデヒドロゲナーゼとグルクロン酸抱合メカニズムを介して5'-カルボン酸と5'-グルクロニドに代謝されます。それは主に尿中に排泄されます-83%(代謝物として;変化しない形で約2%);部分的に糞便で。代謝はラミブジンの除去にほとんど貢献しません。ラミブジンは主に変化せずに尿中に排泄されます。血液中のアバカビルの平均半減期は約1.5時間です。ラミブジン-5-7時間
投与量
口頭で。治療は、HIV感染の管理に経験のある医師が開始する必要があります。大人、青年、子供(25 kg以上):1錠一日一回。患者の特別なグループ。軽度の肝障害(Child-Pughスコア5〜6)の患者では、可能な場合は血中のアバカビルレベルのモニタリングなど、綿密なモニタリングが推奨されます。中等度または重度の肝障害のある患者への使用は推奨されません。 CCr 65歳の患者;腎機能の低下や血液学的パラメーターの変化など、加齢に伴う変化のため、特別な注意が必要です。薬は体重を量る子供に使用されるべきではありません与える方法。薬は食物の有無にかかわらず服用できます。
適応症
成人、青年および子供が体重測定しているヒト免疫不全ウイルス(HIV)感染の治療のための抗レトロウイルス療法の併用≥25kg。アバカビルによる治療を開始する前に、人種的起源に関係なく、HLAB * 5701対立遺伝子の存在のスクリーニングをすべての患者で行う必要があります。アバカビルは、HLA-B * 5701アレルを保有していることが知られている患者には使用しないでください。
禁忌
アバカビル、ラミブジンまたはいずれかの賦形剤に対する過敏症。
予防
生命を脅かす過敏反応は、アバカビルの使用で発生する可能性があります。それらは、複数臓器の変化を示す症状によって特徴付けられます。ほとんどすべての過敏反応は、症候群の一部として発熱や発疹があり、呼吸器症状や消化器症状も含まれる場合があります。アバカビル過敏症反応のリスクは、HLA-B * 5701対立遺伝子が陽性であると診断された患者で高くなりますが、アバカビル過敏症反応は、対立遺伝子を持たない患者でも発生する可能性があります。上記を考慮して、次の推奨事項に従う必要があります。HLA-B* 5701保因者の状態は、治療開始前に常に文書化する必要があります。アバカビルによる治療は、HLA-B * 5701の患者またはHLA-B * 5701のない患者では決して開始すべきではありませんが、以前のアバカビル含有レジメンでアバカビル過敏症反応が疑われます。過敏反応が疑われる場合、HLA-B * 5701対立遺伝子を持たない患者であっても、アバカビル治療は直ちに中止する必要があります(過敏症の発症後の治療中止の遅延により生命に危険が及ぶ可能性があります);過敏反応の疑いがあるためにアバカビルによる治療を中止した後、患者はアバカビルまたは他のアバカビルを含む組み合わせを二度と服用してはなりません(患者は、残っているアバカビル錠剤を破棄するように指示されるべきです)。過敏症反応が疑われる場合にアバカビルを再開すると、数時間以内に症状が急速に戻ることがあります。再発は通常、最初の反応よりも重症であり、命にかかわる血圧の低下や死に至る場合があります。まれに、過敏反応の症状以外の理由でアバカビルを中止した患者も、アバカビル療法を再開してから数時間以内に生命を脅かす反応を経験しました。これらの患者におけるアバカビルの再開は、医療が容易に受けられる環境で行われるべきです。中等度または重度の肝障害のある患者への使用は推奨されません。慢性活動性肝炎を含む肝機能障害の既往がある患者は、抗レトロウイルス療法の併用中に肝機能障害を経験する可能性が高くなります。これらの患者は、認められた診療基準に従って監視されるべきである。そのような患者に肝疾患の悪化の証拠がある場合は、治療の中断または中止を検討する必要があります。抗レトロウイルス療法の併用を受けている慢性B型またはC型肝炎患者は、重篤で致命的な可能性のある肝の有害事象のリスクが高くなります。 B型肝炎ウイルスに同時感染した患者で製剤による治療が中止された場合、ラミブジンの中止により肝炎が急性増悪する可能性があるため、肝機能検査とHBV複製のマーカーの両方を定期的に監視することをお勧めします。アバカビルによる治療と心筋梗塞のリスクとの因果関係は確認または除外できません。アバカビルを処方するときは、修正可能なすべての危険因子(喫煙、高血圧、高脂血症など)を最小限に抑えるための措置を講じる必要があります。プレパレーションでの治療中は、血中脂質とブドウ糖のレベルを監視し、HIV感染の治療に関する以下のガイドラインに従う必要があります。脂質障害は臨床的に適応されたものとして治療されるべきです。併用抗レトロウイルス療法(CART)を開始する患者は、特に治療の最初の数週間または数か月の間、免疫再活性化症候群(無症候性または潜伏日和見病原体に対する炎症反応)の出現を監視する必要があります。炎症のすべての症状は、検査および適用、必要に応じて適切な治療の兆候です。患者、特に進行したHIV疾患の患者および/または長期のCARTユーザーは、骨壊死の兆候である可能性がある関節痛、こわばり、および運動困難などの症状を監視する必要があります(コルチコステロイドの使用、アルコール、重度の免疫抑制、ボディマス指数の増加)。アバカビル/ラミブジンがフマル酸テノホビルジソプロキシルと組み合わせて1日1回投与された初期の段階で、高度なウイルス学的非有効性と急性耐性の報告があります。アバカビルとラミブジンによるウイルス学的失敗のリスクは、他の治療オプションよりも高くなる可能性があります。アバカビル/ラミブジンは、ラミブジンまたはエムトリシタビンを含む他の薬と併用しないでください。ラミブジンとクラドリビンの組み合わせは推奨されません。
望ましくない活動
重度の免疫不全のHIV感染患者は、抗レトロウイルス療法の併用を開始すると、無症候性または残存日和見感染症(免疫再活性化症候群)に対して炎症反応を起こす可能性があります-典型的な例は、全身性および/または局所性サイトメガロウイルス網膜炎ニューモシスチス・カリニによるマイコバクテリア感染症と肺炎;免疫再活性化バセドウ病などの自己免疫疾患も報告されていますが、発症までの時間はさまざまであり、これらのイベントは治療開始後数か月後に発生する可能性があります。骨壊死(頻度は不明)の症例が報告されており、主によく知られた危険因子、進行したHIV疾患、または長期にわたる抗レトロウイルス療法の併用療法を受けている患者に報告されています。抗レトロウイルス療法中に、体重増加、血中脂質、ブドウ糖などの代謝障害が発生することがあります。アバカビル。発疹(通常は黄斑丘疹または蕁麻疹)、吐き気、嘔吐、下痢、腹痛、口内潰瘍、息切れ、咳、喉の痛み、成人呼吸窮迫症候群、呼吸困難などの症状を伴う過敏症(一般) 、発熱、嗜眠、倦怠感、浮腫、リンパ節腫脹、低血圧、結膜炎、アナフィラキシー、頭痛、感覚異常、リンパ球減少症、肝機能検査の上昇、肝炎、肝不全、筋肉痛(まれな筋肉の破壊)、関節痛、CPKレベルの上昇、クレアチニンレベルの上昇、腎不全-過敏反応を発症するほとんどすべての患者は、症候群の一部として発熱および/または発疹(通常は黄斑丘疹または蕁麻疹)を持っていますが、発疹がない場合に反応が起こることがありますまたは発熱。過敏症は致命的な場合があります。一般的:拒食症、頭痛、吐き気、嘔吐、下痢、発疹(全身症状なし)、発熱、嗜眠、疲労。まれ:膵炎(アバカビルとの因果関係は不明)。非常にまれ:乳酸アシドーシス、多形紅斑、スティーブンスジョンソン症候群、中毒性表皮壊死症。ラミブジン。一般的:頭痛、不眠症、咳、鼻の症状、吐き気、嘔吐、腹痛または腹部けいれん、下痢、発疹、脱毛症、関節痛、筋肉障害、疲労、倦怠感、発熱。一般的ではありません:好中球減少症および貧血(両方とも重度の場合があります)、血小板減少症、肝臓酵素(AST、ALT)の一過性の増加。まれ:膵炎、血中アミラーゼの増加、肝炎、血管性浮腫、横紋筋融解症。非常にまれ:赤血球無形成症、乳酸アシドーシス、末梢神経障害(または感覚異常)。
妊娠と授乳
アバカビルとラミブジンは胎盤を通過します。妊娠第1学期にアバカビルを投与された800人を超える患者と、第2および第3学期にアバカビルを投与された1,000人を超える妊婦では、胎児の奇形または胎児への毒性に対するアバカビルの影響の証拠はありませんでした。 )新生児の。最初の学期にラミブジンを服用した1,000人以上の女性と、2番目と3番目の学期にラミブジンを服用した1,000人以上の女性を含む妊娠中の女性では、胎児の奇形または胎児および/または新生児に対する毒性に対するラミブジンの影響の証拠はありませんでした。上記のデータから、人間の奇形のリスクはまずないと思われます。ラミブジンで治療され、その後妊娠するラミブジンと同時感染した患者では、ラミブジンの中止後に肝炎が再発する可能性を考慮すべきです。ヌクレオシドおよびヌクレオチド類似体は、ミトコンドリア機能にさまざまな程度で影響を与える可能性があり、スタブジン、ジダノシンおよびジドブジンで最も顕著です。ミトコンドリア機能障害は、子宮内および/または出生後のヌクレオシド類似体(主にジドブジンを含む治療計画に関連)に曝露された検出不可能なHIV乳児で報告されています。報告された主な副作用は、血液障害(貧血、好中球減少症)、代謝障害(乳酸過剰、リパーゼレベルの上昇)、あまり一般的ではない神経障害(筋肉緊張の増加、けいれん、行動障害)でした。上記の結果は、子宮内で病因が不明である重篤な臨床症状、特に神経学的症状のある準備に子宮内で曝された子供に対して考慮されるべきです。これらの結果は、HIVの垂直な母子感染を防ぐために妊婦に抗レトロウイルス療法を使用するための現在の推奨を拒否する根拠にはなりません。アバカビルとラミブジンは母乳中に排泄されます。 HIV感染を避けるために、HIV感染女性はいかなる状況でも乳児に母乳を与えないことが推奨されます。アバカビルとラミブジンは生殖能力に影響を与えませんでした(動物研究)。
コメント
機械を運転して使用する決定は、患者の臨床状態と起こり得る副作用を考慮に入れるべきです。
相互作用
アバカビルとラミブジンは、CYP3A4、CYP2C9、CYP2D6などのチトクロームP450酵素によって有意に代謝されません。それらはこれらのアイソザイムのインデューサーまたはインヒビターでもありません-抗レトロウイルスプロテアーゼインヒビター、非ヌクレオシドおよびP450酵素によって代謝される他の薬物との相互作用のリスクはありそうもありません。アバカビルとラミブジンの間に臨床的に関連のある相互作用は示されていません。アバカビル。アバカビルは、UDP-グルクロニルトランスフェラーゼ(UGT)とアルコール脱水素酵素によって代謝されます。 UGT酵素を増強または阻害する薬物、またはアルコール脱水素酵素によって排除される薬物を同時に投与すると、アバカビルへの曝露が変わる可能性があります。ジダノシンまたはジドブジンと併用した場合、用量調整は必要ありません。 UGTに対する作用のため、リファンピシン、フェノバルビタール、フェニトインなどの強力な酵素誘導剤は、アバカビルの血中濃度をわずかに低下させる可能性があります。用量変更の推奨を行うにはデータが不十分です。フェニトインと併用する場合、血中濃度を監視する必要があります。アバカビルの代謝は、アルコールの同時投与(アルコールデヒドロゲナーゼの阻害)によって変化します-アバカビルのAUCは、これらの症例で約41%増加します。これらの所見は臨床的に関連があるとは見なされず、用量調整は必要ありません。アバカビルはアルコール代謝に影響を与えません。レチノイドはアルコール脱水素酵素を介して排除され、アバカビルとの相互作用は可能ですが研究されていません。用量変更の推奨を行うにはデータが不十分です。メタドンは、1日2回600 mgの用量でアバカビルと同時投与された場合、アバカビルCmaxを35%削減しますが、AUCは変更されません(アバカビルの薬物動態のこの変化は臨床的に関連しません)。アバカビルは、メタドンの平均クリアランスを22%増加させます。アバカビルの用量調整は必要ありません。同様に、ほとんどの患者はメタドンの用量調整を必要とする可能性は低く、一部のメタドンの用量調整が必要になる場合があります。ラミブジン。ラミブジンは腎臓から排泄されます。ラミブジンの尿への活発な腎分泌は、有機カチオン担体(OCT)の関与により溶出されます。ラミブジンとOCT阻害剤の同時投与は、ラミブジン暴露を増加させる可能性があります。コトリモキサゾール(スルファメトキサゾールを含むトリメトプリム)は、ラミブジンAUC(OCT活性の阻害)を増加させます。ラミブジンはコトリモキサゾールの薬物動態に影響を与えません-患者が腎障害の症状を発現するまでラミブジンの用量調整は必要ありませんが、患者を監視する必要があります。ニューモシスチス・カリニ肺炎(PCP)およびトキソプラズマ症の治療に使用される高用量のコトリモキサゾールを用いたラミブジンの投与は避けるべきです。シメチジンとラニチジンはこのメカニズムによって部分的にしか排泄されず、ラミブジンとの臨床的に重要な相互作用はありそうもありません-用量調整は必要ありません。ジドブジンのようなヌクレオシド類似体(例えば、ジダノシン)はこのメカニズムによって排泄されないため、ラミブジンとの相互作用は起こりそうにありません-用量調整は必要ありません。類似性のため、ラミブジンはエムトリシタビンなどの他のシチジン類似体と併用して投与すべきではありません。さらに、ラミブジンを含む他の薬物と同時に準備をするべきではありません。ラミブジンは、クラドリビンの細胞内リン酸化を阻害します。これにより、クラドリビンの有効性が失われる可能性があります。ラミブジンとクラドリビンの併用は推奨されません。
準備には物質が含まれています:ラミブジン、アバカビル
償還された薬物:いいえ