チロシンキナーゼ阻害剤は、がんの治療に使用される薬です。このグループの物質の作用は、特定の種類の酵素であるチロシンキナーゼの遮断に基づいています。過去30年間の研究では、これらの酵素が腫瘍性病変内で活性の増加を示すことが示されています。チロシンキナーゼ阻害剤は、がん細胞に対する標的治療に使用されます。
目次
- がん薬物療法とは?
- 腫瘍性変化はどのように発生しますか?
- チロシンキナーゼの機能は何ですか?
- チロシンキナーゼの機能への損傷の影響は何ですか?
- チロシンキナーゼ阻害剤はどのように機能しますか?
- 非受容体型チロシンキナーゼ阻害剤
- 受容体チロシンキナーゼ阻害剤
- チロシンキナーゼ阻害剤の副作用
チロシンキナーゼ阻害剤(TKI)は、分子標的化され、癌の治療に使用される薬物のグループに属しています。標的療法の一部として使用した場合、それらは選択的に作用し、副作用が大幅に少なくなります。
がん薬物療法とは?
腫瘍性変化の薬理学的治療の主な方法は化学療法です。損傷の結果として、癌細胞は無限に分裂する可能性があります。彼らはまた、自然細胞死プログラム、またはアポトーシスの対象ではありません。このグループの薬物の作用機序は、細胞分裂の阻止とそれらの死の開始に基づいています。
化学療法の主な問題は、細胞増殖抑制薬が罹患した細胞と健康な細胞の両方に毒性があることです。彼らは体全体の細胞分裂をブロックします。それらは特に、骨髄などの新しい細胞が大量に生成される組織を損傷します。このメカニズムは、化学療法の深刻な副作用の原因です。
現在、新しい抗がん剤の探索は、がん細胞にできるだけ有害であり、健康なものを破壊しない物質に焦点を当てています。分子生物学の分野における大きな進歩のおかげで、古典的な細胞増殖抑制剤とは異なる働きをする薬物を作成することが可能になりました。この新しいアプローチは、標的療法と呼ばれています。
標的療法は、がん細胞の分裂を刺激する信号が送信される方法をブロックすることによって機能します。それは細胞分裂自体ではなく、情報伝達への特定の損傷に焦点を合わせています。このアプローチのおかげで、新薬は従来の細胞増殖抑制剤よりも癌細胞に対してより選択的です。そのような製剤はチロシンキナーゼ阻害剤である。
腫瘍性変化はどのように発生しますか?
がん細胞は、DNAの変異の結果として発生します。つまり、適切な機能に関する情報を含む遺伝物質です。ただし、その損傷のすべてが癌の形成につながるわけではありません。変更は、ライフサイクル情報と分割に関するものでなければなりません。健康な細胞は、必要な信号を受け取ると分裂します。それらが損傷している場合、それらはアポトーシス、またはプログラムされた死を受けます。癌細胞にはこの調節がないため、制御不能に分裂します。
DNA変異は、自然発生的に自然発生する可能性があります。ただし、腫瘍性変化は、ほとんどの場合、外的要因によって引き起こされます。これらは、化学的変異原、すなわち遺伝物質に影響を与えるさまざまな種類の毒物である可能性があります。たとえば、そのような毒素はタバコの煙に含まれています。物理的な変異原もあります。このグループには、UVなどのさまざまなタイプの放射線が含まれます。
発癌性ウイルスは、腫瘍性変化を引き起こす能力もあります。これは、人間の細胞での増殖の仕方によるものです。ウイルスは遺伝物質を私たちのDNAに導入し、変化を引き起こします。研究により、これらの修飾がチロシンキナーゼの合成に時々あることが示されています。これらのタイプの変化は、細胞分裂のサイクルに対する身体の制御を妨害します。
チロシンキナーゼの機能は何ですか?
チロシンキナーゼは、調節タンパク質として機能する酵素です。これらは、成長、運動、分裂など、細胞の基本的な機能に関する情報を送信するために使用されます。変異によって損傷したチロシンキナーゼは誤った情報を送り、腫瘍性変化の形成につながります。
これらの酵素は、細胞膜にある受容体キナーゼと細胞内にある細胞質キナーゼの2つのグループに分類できます。膜にある受容体タンパク質は、細胞に付着する化学分子の形で細胞外から情報を受け取ります。そのような情報は、例えば、細胞分裂を開始するための呼び出しであり得る。
細胞内チロシンキナーゼは、受容体タンパク質から細胞へのシグナル伝達に関与しています。キナーゼの刺激は、核へのシグナル伝達につながるタンパク質カスケードを引き起こします。これが細胞分裂の開始に関する情報である場合、以前は受容体キナーゼによって刺激されていた細胞質キナーゼによって伝達された後に開始されます。この規制システムは、体内のすべての健康な細胞がスムーズに機能することを保証します。
チロシンキナーゼの機能への損傷の影響は何ですか?
突然変異の結果として、細胞内で情報を伝達するこの方法は妨げられる可能性があります。変異型チロシンキナーゼは、細胞分裂の開始に関する情報を継続的に伝えます。それらはシグナル伝達分子によって調節されていません。これにより、制御されない細胞増殖が起こり、その結果、腫瘍性変化が形成されます。
白血病を含む多くの悪性腫瘍は、チロシンキナーゼの増加した活性を示すことが示されています。これらの腫瘍性病変の変異タンパク質は、シグナルを過度に吸収および伝達します。これは、増殖やプログラムされた死などの細胞プロセスの混乱につながります。
調節不全はまた、酵素の自己分泌活性化を介して発生する可能性があります。間違いのため、チロシンキナーゼはそれ自身のアクチベータータンパク質の合成を刺激します。このタンパク質は、アクチベーター合成を再刺激するキナーゼを活性化します。これにより、自己強化反応ループが作成されます。チロシンキナーゼの機能におけるこの種のエラーは、とりわけ乳癌、卵巣癌、膀胱癌、および脳癌で観察されています。
チロシンキナーゼ阻害剤はどのように機能しますか?
チロシンキナーゼ阻害剤の作用機序は、酵素の活性部位へのこれらの薬物の付着に基づいています。したがって、薬物はチロシンキナーゼの活性化をブロックします。その結果、新しい部門の開始に関するカーネルへの情報の送信が停止します。
チロシンキナーゼ阻害剤は効果的な薬です。それらは腫瘍細胞に対して選択性を示し、そのおかげで古典的な細胞増殖抑制薬よりも副作用が少ない。これらの薬の利点は、それらのほとんどが経口であるということでもあります。これにより、入院の快適さが増し、静脈内投与に関連する合併症がなくなります。使用の安全性と相乗効果により、従来の細胞増殖抑制剤との併用に適しています。
チロシンキナーゼ阻害剤は現在、癌治療に成功裏に使用されています。このグループの新薬の研究はまだ進行中です。多くのチロシンキナーゼ阻害剤が臨床開発中である。
チロシンキナーゼ阻害剤は、非受容体薬と受容体薬に分けられます。
非受容体型チロシンキナーゼ阻害剤
このグループの薬剤は、慢性骨髄性白血病および急性リンパ性白血病の癌細胞に対して特に有効です。この治療グループには以下が含まれます:
- イマチニブ-チロシンキナーゼの活性を阻害する最初に承認された薬物。白血病および消化管の手術不能のがんの治療に使用されます。イマチニブによる治療は、比較的低い毒性で高い割合の寛解を達成します。この薬による治療の最大の問題は耐性です。治療中に発症することもありますが、一部の患者では腫瘍性病変がイマチニブに対して一次耐性を示すこともあります。これは、初めて治療を受ける患者の20-30%に適用されます
- ダサチニブ-イマチニブ耐性の症例の慢性骨髄性白血病の治療に使用されます
- nilotinib-イマチニブ耐性でも使用
受容体チロシンキナーゼ阻害剤
このグループの薬には、細胞膜の表面にある受容体キナーゼの阻害剤が含まれます。阻害剤が作用する受容体のタイプに応じて、それは3つのタイプに分けることができます:
上皮成長因子受容体阻害剤は、大腸癌、子宮頸癌、肺癌、前立腺癌などの悪性新生物の治療に使用されます。
このカテゴリには以下が含まれます:
- ゲフィチニブ
- エルロチニブ
- ラパチニブ
血管内皮増殖因子受容体阻害剤は、腫瘍性病変における新しい血管の形成をブロックします。ほとんどすべての腫瘍性腫瘍は、酸素欠乏に反応して血管内皮増殖因子を分泌します。それは新生物領域の血管の形成を刺激します。これにより、腫瘍の酸素化とさらなる拡大が可能になります。適切なチロシンキナーゼの阻害剤を使用することにより、このプロセスをブロックすることができます。このグループの薬には、
- セマキシニブ
- バラタニブ
- スニチニブ
- ソラフェニブ
血小板増殖因子受容体阻害剤は、骨髄性白血病、神経膠芽腫、および他の多くの癌の治療に使用されます。それらはまた関節リウマチの免疫抑制剤として使用されます。このグループには以下が含まれます:
タンデュチニブ
レフルノミド
チロシンキナーゼ阻害剤の副作用
これらの薬の副作用は70%以上の患者に見られます。幸いにも、それらは通常中程度から穏やかな強度レベルを持っています。間質性肺炎は治療の深刻な合併症ですが、非常にまれにしか発生しません。
最も一般的な副作用:
- 下痢
- 皮膚の変化
- 弱点
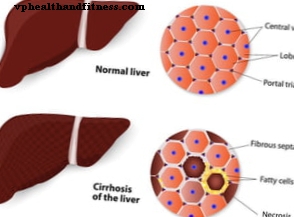
- 肝機能障害
文献
- PłużańskiA、Piorek A.チロシンキナーゼ阻害剤の副作用-管理ガイドライン。 Oncol Clin Pract 2016; 12:113-118。 DOI:10.5603 / OCP.2016.0004。オンラインアクセス
- 抗癌療法におけるチロシンキナーゼ阻害剤-抗癌療法におけるチロシンキナーゼ阻害剤、KatarzynaSobańska、EdytaSzałek、AgnieszkaKamińska、EdmundGrześkowiak、FARMACJAWSPÓŁCZESNA2011; 4:185-190、オンラインアクセス
- チロシンキナーゼ-抗癌療法の新しい目標、Ireneusz Majsterek、Dariusz Pytel、JanuszBłasiak、PostępyBiochemii、オンラインアクセス

この著者による他の記事を読む








.jpg)



---zastosowanie-dziaanie-skutki-uboczne.jpg)