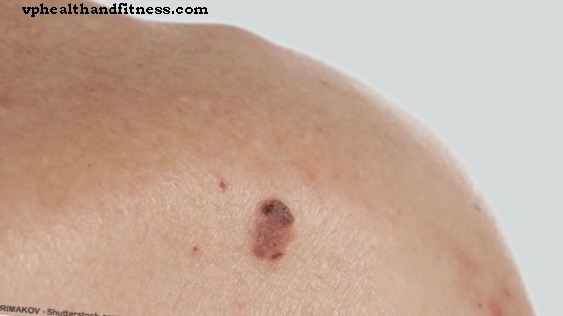
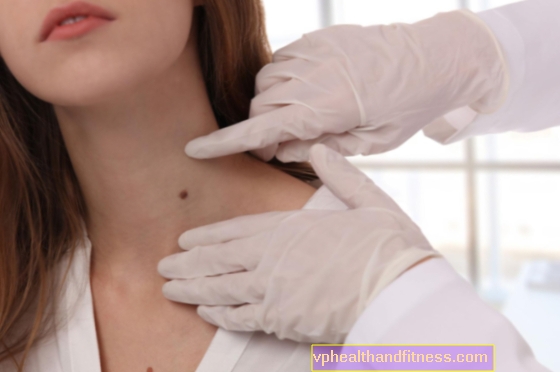
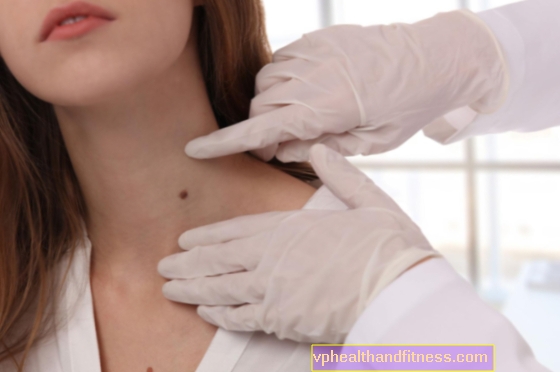
線維素溶解は、恒常性の一部としての血栓溶解の生理学的プロセスであり、多くの酵素の活性化によって引き起こされます。このプロセスは、血管の開存性を維持し、血管新生、創傷治癒、腫瘍成長および転移形成において役割を果たす。
目次
- 線溶-コース
- 抗線溶メカニズム
- 線維素溶解の障害
線溶は、凝固に対抗する生理学的プロセスです。どうして?血栓を溶かすからです。
線溶-コース
線溶酵素プラスミンは血漿中を循環します。プラスミンはフィブリン、フィブリノーゲン、血漿因子を分解します:V、VIIIおよびXIIおよびプロトロンビン。プラスミンは、組織のプラスミノーゲン活性化因子(t-PA)およびウロキナーゼ型のプラスミノーゲン活性化因子(u-PA)の影響下で、不活性なプロ酵素-プラスミノーゲンから生成されます。プラスミノーゲンのプラスミンへの変換は、トロンビンが原因で発生することもあります。
組織プラスミノーゲン活性化因子とウロキナーゼプラスミノーゲン活性化因子は、内皮(t-PA)や腎臓(u-PA)を含むさまざまな細胞や臓器で産生されます。それらは、カリクレインまたはプラスミンによって活性な二本鎖型に変換される一本鎖前駆体の形で形成されます。 XII因子の血漿分解産物は、血管を拡張するキニンの生成を活性化します。
T-PAは、主にフィブリンの溶解、したがって血管を開いた状態に保つために重要です。一方、u-PAが関与して形成されるプラスミンは、いわゆるメタロプロテイナーゼ(タンパク質分解酵素のグループ)は、組織のリモデリングと細胞移動(血管新生につながり、創傷の治癒、腫瘍の成長と転移の形成に役立ちます)で役割を果たします。
抗線溶メカニズム
プラスミノーゲン活性化因子の2つの阻害剤があります:PAI-1とPAI-2-これらは、巨核球、肝臓と内皮細胞(PAI-1)だけでなく、胎盤、単球(PAI-2)でも産生されるタンパク質です。彼らはわずかに異なる行動メカニズムで異なります。血漿中に含まれる物質は、肝臓で産生される物質であるα2-アンチプラスミンです。血漿アルファ2アンチプラスミンが枯渇すると、プラスミンはアルファ2マクログロブリンによって中和されます。
別の線溶阻害剤-プロカルボキシペプチダーゼB2はトロンビン(TAFI)によって活性化されます
プラスミンによるフィブリンとフィブリノーゲンの分解の過程で、分解生成物が形成されます-フラグメントX、Y、D、E架橋フィブリンのプラスミン消化中に、フラグメントDの代わりに、ダイマーDが形成されます-静脈血栓塞栓症の診断プロセスで役割を果たす重要な診断マーカーです。限界値は実験室によって異なります。最も頻繁に報告される500ng / mlの値は、それ以下ではVTEが起こりそうにない限界です。
線維素溶解の障害
線溶障害は進行するか、このプロセスを弱めます。
先天性出血素因は、特に、線溶の増加した活動について血管壁が損傷した後は、血餅が非常に速く溶解するため、出血を制御するのは困難です。線溶阻害剤は症状を緩和するために使用されます。
線維素溶解のプロセスは、播種性血管内凝固症候群(DIC)でも妨げられます。これは、次のような多くの臨床症状に続発する症候群です。
- 敗血症
- 広範なトラウマ
- 急性膵炎
- 悪性腫瘍
血液凝固プロセスの一般化された活性化、および線溶プロセスの活性化または阻害からなる。微小循環に複数の血栓が形成され、多くの臓器の虚血を引き起こします。血小板、フィブリノーゲン、血漿凝固因子の消費は、出血素因によって現れます。
以下のような特定の病状では:
- 虚血性脳卒中
- 心筋梗塞
- 肺塞栓症
基質は血栓による血管内腔の閉鎖です。
いくつかのケースでの救命療法の主力は、線溶剤を使用した血栓溶解です。線溶薬には、ウロキナーゼ、アルテプラーゼ、ストレプトキナーゼなどがあります。これらの薬は輸液として静脈内投与されます。
ほとんどの場合、症状の発症から診断、薬物投与までの時間は、人の人生にとって決定的な価値があります。